- Forklar hvorfor cellemembraner utgjør en diffusjonsbarriere for enkelte typer molekyler men ikke andre.
Fordi cellemembranen består av et dobbelt lipidlag og er lite gjennomtrengelig for b.la. polare molekyler. Det er derfor membranen trenger porer og kanaler for ioner, vann, store makromolekyler usw. - Gi eksempler på hvilke transportmekanismer som kan regulere cellens pH. Til kasuistikken:
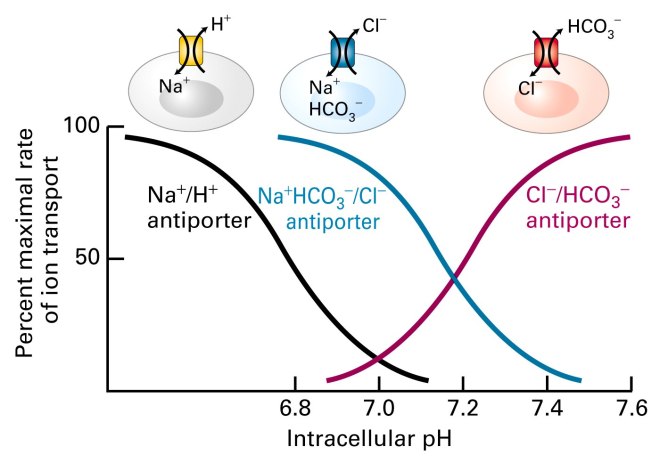
– Na+/H+ antiportør
– Na+HCO3-/Cl- antiportør
– Cl-/HCO3- antiportør
- Hvilke konsekvenser ville det ha dersom de tilførte væskene hadde annen osmolalitet enn den fysiologiske?
Væsken hadde forstyrret det osmotiske trykket (høyere osmolalitet: lekke ut, lavere osmolalitet: lekke inn). - Hva er hensikten med å gi albumin?
Albumin gjør at væsken holdes inne i blodårene. Det er viktig å opprettholde kroppens osmotiske trykk sånn at plasma ikke diffunderer inn i kroppen. Hvorfor vente til dag to? På dag en er porene i blodåremembranene så store at alt som renner inn i kroppen kommer til å renne ut igjen. Da er det først og fremst viktig å erstatte tapt natrium og holde pasienten hydrert. Det osmotiske trykket består ikke bare av ioner, men også proteiner usw.
Oppbygning av cellens membraner
- Dobbelt fosfolipidlag (e.g. glycolipider, sfingolipider)
- Proteiner
- Porer
E.g. akvaporiner - Kanaler
- Kolesterol
Kolesterol gjør at lipidmembranen blir mer rigid og dermed elastisk; elastiske materialer er et stadie mellom de flytende og faste - Lipid drafts
Områder med mye kolesterol og er viktig for å bl.a. regulere bevegelsen av membranproteiner - Glykolipidlag
Utenpå cellemembranen. Beskytter mot farlige endringer i pH. Viktig også for cellesignalisering
Transportprosesser for ulike molekyler over cellemembranen
Passive mekanismer
- Diffusjon
- Fasilitert diffusjon (ved bærermolekyler)
Med konsentrasjonsgradient
Aktive mekanismer
- Primærtransport
Virker mot konsentrasjonsgradienten - Sekundærtransport
Symport: molekyler utnytter en åpning som allerede eksisterer (mindre resistanse)
Antiport: et molekyl beveger seg med konsentrasjonsgradienten (passivt), mens et annet bruker åpningen til å bevege seg mot den
Endo(inn)cytose og ekso(ut)cytose
Årsakene til at det er en skjevfordeling av ioner over cellemembranen
Ujevn fordeling av lekkende ionekanaler. Lipidmembranen er en god isolator. Ioner trenger derfor kanaler eller transportører for å komme seg gjennom.
Osmotiske krefter og cellens volumkontroll
Akvaporiner er med på å regulere vanninnholdet i en celle. Eksperiment: et froskeegg som er genmanipulert til å ha flere akvaporiner i cellemembranen vil svelle unormalt mye i vann.
Cellers pH-regulering og bufferkapasitet
To måter (Avhengig / Uavhengig av Na+)
- H+ ut
Na+/H+-antiportør. Na+ pumpes inn og H+ ut. - Bikarbonat (base) inn
Cl- ut. NaHCO3 inn. Na+ frigjøres. HCO3- binder seg til H+ i lumen og danner H2CO3 (karbonsyre) som igjen kan reagere videre til H2O og CO2.
Uavhengig av Na+
Antiport: Cl- inn og HCO3- ut (for å utjevne alkalinitet).
H+ produseres i cellen hele tiden. HCO3 tar opp H+. Når bikarbonatkonsentrasjonen faller, begynner H+ å binde seg hyppigere med OH-.
Lysosomer
H+ kan pumpes inn i lysosomer ved primærtransport (energikrevende, ATP). pH i et lysosom er ~5. I cytosol er pH ~7.2.
Faktorer som bestemmer transporthastigheten av molekyler over korte avstander, samt de vanligste transportveier gjennom membranen
- Avstand
- Brownske bevegelser
- Affinitet
- Størrelse
- Stoffkonsentrasjoner
- Membranens overflate
Usw.
Syre/base, buffere og eksempler på pH-forstyrrelser (acidose)
Ved nyresvikt vil syreholdig urea usw. bli værende i kroppen. Laktat, H+-nivået går opp o glikevekten forskyves. pH i blodet øker. Den naturlige reaksjonen er å hyperventilere, men det er ikke nok i seg selv.
Foreleser: Laura Trachsel Moncho
Oppgaver
Ressurser

