Dyspné
Dyspnoé er en subjektiv opplevelse av pustebesvær hos pasienter med sykdom i lunger og/eller andre organer som påvirker respirasjonssystemet. Det er ofte lite samsvar mellom pasientens opplevelse og de objektive funn. Dyspnoé er ofte anstrengelsesutløst og forsterkes av angst.
Ekspektorat
Ekspektorasjon er oppspytt fra de nedre luftveiene. Ekspektoratet inneholder sekret fra bronkialtreet, celler, cellerester og eventuelle partikler som er inhalert og spytt. Å ekspektorere er den medisinske betegnelsen på å hoste opp.
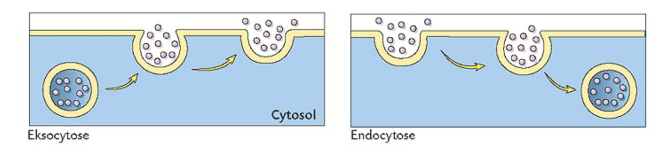
Ventilasjon
Ventilasjon er transport av luft inn og ut av lungene. Et åndedrett består av innånding (inspirasjon) og utånding (ekspirasjon).
Sentral cyanose
Sentral cyanose er en tilstand der tunge og lepper blir blålige. Dette skyldes oftest hypoksemi, som igjen skyldes sykdommer i hjerte eller lunge; men kan også skyldes ekstrem kulde eller andre forhold.
Perkusjon
Perkusjonen utføres ved å tromme på pasientens rygg og brystkasse og lytte etter lydkvaliteten, omtrent som når en tømrer banker på veggen for å høre hvor det er spikerslag. Målet er å finne lungegrensene og lungenes “tetthet”. Perkusjon kan gi en pekepinn på lungegrensene og om det er dempning eller hypersonorperkusjonslyd.
Auskultasjon
Ved auskultasjon forsøker man å avgjøre kvaliteten på auskultasjonslydene ved hjelp av et stetoskop. Man lytter både etter selve respirasjonslyden og etter eventuelle fremmedlyder. Altså at man lytter på organer med stetoskop.
Respirasjonslyden
Respirasjonslyden beskrives gjerne som normal, svekket eller økt (såkalt bronkial blåst), og det er viktig å angi variasjoner i respirasjonslydene over alle lungeflatene. Fremmedlyder angis gjerne som pipelyder, knatrelyder eller gnidningslyder.
Krepitasjon
Krepitasjon, knatrelyder som høres over lungene når man lytter med stetoskop. Se knatrelyder, auskultasjon. Skyldes væske i alveolene. Små bobler som kommer til overflaten og knitrer.
Den venstre lungen, som er noe mindre enn den høyre, har to lapper: en øvre lapp (lobus superior) og en nedre lapp (lobus inferior). Den høyre lungen har i tillegg til den øvre og nedre også en midtlapp (lobus medius).
Lungebetennelse, pneumoni på fagspråket, er en betennelse i lungevevet som følge av en infeksjon med bakterier eller virus. Lungevevet vil si lungeblærene (alveolene), der den livsviktige transporten av oksygen fra luft til blod foregår. Når lungevevet blir betent, kan det bli tyngre å puste. Jo mer omfattende lungebetennelsen er, jo tyngre blir det å puste.
Ikke all innpustet luft kommer ned i alveolene. Om lag 150 ml av hvert tidevolum strømmer bare ned i de delene av luftveiene hvor det ikke skjer gassveksling mellom luft og blod, og som kalles det anatomiske dødrom (VD). Vanligvis er det den alveolære ventilasjonen (VA) man er interessert i. Den defineres som differansen mellom tidevolum og dødrom multiplisert med pustefrekvensen: VA=f(VT–VD). Volumet per tidsaspekt. Det er bare gassfasen, ikke det som absorberes inn i blodet som medregnes.
Dødrommet
Respirasjonsystemet har “dødrom” i munnhulen og alle åpningene til lungene (og nederste del av lungene).
Tachykardi
Rask puls
Hvorfor krever det energi å inspirere?
Luft vil gå fra områder med høyt trykk til områder med lavt trykk (for å utjevne trykkforskjeller). Når vi puster inn må vi lage undertrykk i lungene for å få inn luft. Den aktive delen i dette arbeidet er diafragmaen (som går bra buet til rett). Et elastisk bindevevslag trekker lungene tilbake. Ryggbeina fungerer som bøttehank. Når lungene ekspanderer går de ut til siden og det blir større diameter.
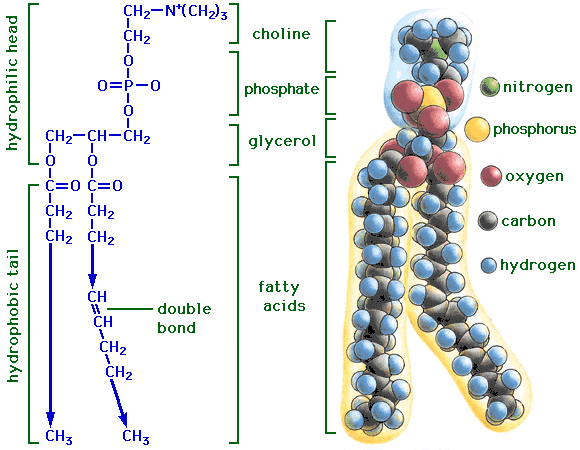
Oksygen transporteres i hemoglobin.
Respirasjonssenter og regulatorer
I kroppen er det flere grupper nevroner som regulerer respirasjonen. De finnes i både forlenget marg og pons (hjernebroen). Kjemosentrene måler arterieblodet til hjernen.
Det er flere grupper nevroner. Finnes både i forlenget marg og pons (hjernebroen). O2, CO2, pH → sentrale kjemosentrene måler arterieblodet til hjernen. Aortabuen, kariotearteriene (halsarteriene). Mest kjente perifere. Sinus kariotikus (kjemoreseptor), globus kariotikus, aortalegemene.
Hjertet består av muskelvev med evne til å lede og generere strøm. Det er en egen type muskelcelle som er ulik skjelettmuskelcelle og glattmuskelcelle (tverrstripet riktig nok). Etter arteriene deler de seg inn i arterioler og kapillærer.
Kretsløp i kroppen:
- Lungekretsløp
Lille
Kroppskretsløp
Store
Blodtrykk
- Systolisk
Hjertet trekkes sammen og har en kontraksjon
- Diastolisk
Hjertet er i ro og fylles
Hvordan reguleres blodtrykket når vi reiser oss? Hvorfor hender det at vi besvimer? Det som skjer er at vi opplever et statisk blodtrykksfall (mangel på blodvolum). Kroppen har ikke fått trykket nok opp til å gjennomblø hjernen i stående stilling (gravitasjon virker fra hjernen og ned). Minuttvolum = frekvens * slagvolum. Vi har klaffer i venene som styrer retning og strøm. Når vi måler blodtrykk måler vi det arterielle.
Fysiologiske mekanismer
- Hurtig puls
Adrenalin
- Blekhet
Sympatisk nervesystem aktiveres og gjør at blodårene trekker seg sammen
Hvor i kroppen registreres blodtrykksfall?
Aortabuen og halsarterien. De reagerer på strekk, et indirekte mål på blodtrykket.
Prinsippene bak reabsorpsjon i tubulus:
Natrium-kalium-pumpen(atpase) pumper Na+ og K+ ut av cellen og inn i kapillæren. Da blir det lav saltkonsentrasjon i cellen. Na+ og K+ fra tubulus går da inn i cellen (sammen med vann). Sukker og aminosyre absorberes ved aktiv transport. Natrium-kalium-atpase brukes som drivkraft til natrium-glukose-kotransportør.
ADH regulerer væske- og elektrolyttbalanse (ioner). Hormonet aldosteron fra binyrebarken gir flere natrium- og kaliumkanaler som styrker natrium-kalium-pumpen.
Foreleser: Johan Frederik Storm
Ressurser
Oppgaver